Dichlore
| Dichlore | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||

| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Dichlore dans une ampoule. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Identification | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| Nom UICPA | dichlore | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| No CAS | 7782-50-5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| No ECHA | 100.029.053 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| No CE | 231-959-5 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| No E | E925 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Apparence | gaz jaune-verdâtre, d'odeur âcre | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriétés chimiques | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Formule | Cl2 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Masse molaire | 70,906 ± 0,004 g/mol Cl 100 %, |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriétés physiques | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T° fusion | −101 °C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| T° ébullition | −34,6 °C | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Solubilité | 14,6 g l−1 dans l'eau à 0 °C, 7,3 g l−1 à 20 °C, 5,7 g l−1 à 30 °C |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
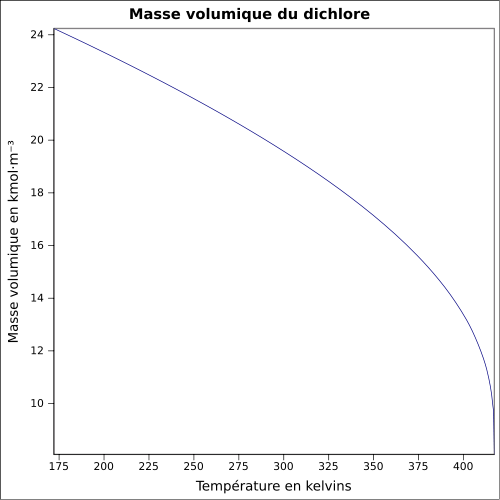
| Masse volumique | 2,48 (densité par rapport à l'air) à 20 °C, 6,864 atm : 1,408 5 g cm−3 (liq.) à −35 °C, 0,994 9 atm : 1,564 9 g cm−3 (liq.) équation :
ρ
=
2.23
/
0.27645
(
1
+
(
1
−
T
/
417.15
)
0.2926
)
{\displaystyle \rho =2.23/0.27645^{(1+(1-T/417.15)^{0.2926})}}
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
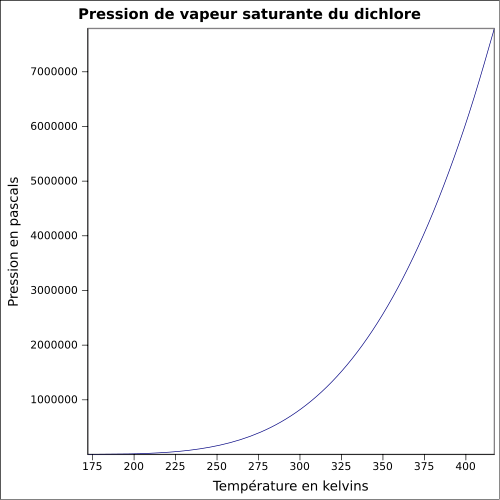
| Pression de vapeur saturante | 6,776 bar à 20 °C 8,8 bar à 30 °C 14,3 bar à 50 °C équation :
P
v
s
=
e
x
p
(
71.334
+
−
3855
T
+
(
−
8.5171
)
×
l
n
(
T
)
+
(
1.2378
E
−
2
)
×
T
1
)
{\displaystyle P_{vs}=exp(71.334+{\frac {-3855}{T}}+(-8.5171)\times ln(T)+(1.2378E-2)\times T^{1})}
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Point critique | 143,81 °C 79,914 bar 0,576 88 kg l−1 |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Point triple | −100,98 °C 0,013 87 bar |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Vitesse du son | 206 m s−1 (0 °C, 1 atm) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Thermochimie | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ΔvapH° | 20,41 kJ mol−1 (1 atm, −34,04 °C) ; |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cp |
équation :
C
P
=
(
6.3936
E
4
)
+
(
46.350
)
×
T
+
(
−
0.16230
)
×
T
2
{\displaystyle C_{P}=(6.3936E4)+(46.350)\times T+(-0.16230)\times T^{2}}
|
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Propriétés électroniques | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 1re énergie d'ionisation | 11,480 ± 0,005 eV (gaz) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Cristallographie | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Symbole de Pearson | o C 8 {\displaystyle oC8\,} | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Classe cristalline ou groupe d’espace | Cmca (no 64) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Strukturbericht | A14 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Structure type | I2 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Précautions | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SGH | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
    DangerH270, H315, H319, H330, H335 et H400H270 : Peut provoquer ou aggraver un incendie ; comburant H315 : Provoque une irritation cutanée H319 : Provoque une sévère irritation des yeux H330 : Mortel par inhalation H335 : Peut irriter les voies respiratoires H400 : Très toxique pour les organismes aquatiques |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| SIMDUT | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
   A, D1A, E, A : Gaz comprimé tension de vapeur absolue à 50 °C =750 kPa D1A : Matière très toxique ayant des effets immédiats graves Transport des marchandises dangereuses : classe 2.3 E : Matière corrosive Transport des marchandises dangereuses : classe 8 Divulgation à 1,0 % selon la liste de divulgation des ingrédients Commentaires : tel que présenté dans l'interprétation d'une politique de santé Canada, le symbole de danger D1 (tête de mort) n'a pas à apparaître sur l'étiquette du fournisseur. Cependant, tous les dangers pour la santé et la sécurité que présentent ce produit doivent être divulgués sur l'étiquette et la fiche signalétique. |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| NFPA 704 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 040OX | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Transport | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
265 : gaz toxique et comburant (favorise l'incendie) Numéro ONU : 1017 : CHLORE Classe : 2.3 Code de classification : 2TOC : Gaz liquéfié, toxique, comburant, corrosif. Étiquettes :  2.3 : Gaz toxiques (correspond aux groupes désignés par un T majuscule, c'est-à-dire T, TF, TC, TO, TFC et TOC).  5.1 : Matières comburantes  8 : Matières corrosives |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Inhalation | odeur suffocante | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Écotoxicologie | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CL50 | 1 heure : rat 293 ppm souris 137 ppm |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Seuil de l’odorat | bas : 0,02 ppm haut : 3,4 ppm |
||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| Unités du SI et CNTP, sauf indication contraire. | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| modifier |
|||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
Le dichlore (Cl2) est un gaz jaune-vert (chloros signifie « vert » en grec) dans les conditions normales de température et de pression. Il est 2,5 fois plus dense que l'air. Il a une odeur suffocante très désagréable et est extrêmement toxique car il se recombine avec l'humidité des muqueuses et des poumons pour former des acides qui attaquent les tissus.
Le dichlore a été découvert par Carl Wilhelm Scheele en 1774. Il a été utilisé lors de la Première Guerre mondiale en tant que gaz de combat, la bertholite.
Le dichlore est soluble dans l'eau, formant l'eau de chlore, mais il n'est pas soluble dans l'eau salée.
La molécule de dichlore est formée de deux atomes de chlore.
Production
Le dichlore peut être produit facilement en électrolysant une solution de chlorure de sodium (procédé chlore-alcali) :
2Na+ + 2Cl− + 2H2O → 2NaOH + Cl2 + H2.Scheele le synthétisa en faisant réagir du dioxyde de manganèse (MnO2) avec de l'acide chlorhydrique (HCl).
On peut également en fabriquer de petites quantités grâce à la réaction de l'acide chlorhydrique sur le permanganate de potassium.
De plus, quand on verse un acide dans de l'eau de Javel, on observe une libération de dichlore (mais en présence d'urée, présent dans l'urine, elle dégage de la trichloramine (NCl3) ; gaz très irritant). Le degré chlorométrique d'une solution de Javel est le volume de dichlore libéré par un litre de cette solution (acide en excès).
Cl− + ClO− + 2H+ → Cl2 + H2OUtilisation
Le dichlore est utilisé comme matière première pour produire de l'acide chlorhydrique par réaction entre le dichlore et le dihydrogène.
Cl2 + H2 → 2HClIl est aussi utilisé pour produire du polychlorure de vinyle (PVC).
Il sert dans la fabrication des produits avec une liaison carbone-chlore comme le fluide frigorigène R12 dichlorodifluorométhane.
Il sert aussi à désinfecter l'eau potable en remplacement de l'eau de Javel.
Il a été utilisé comme gaz de combat (car irritant pour les voies respiratoires supérieures et toxique) pendant la Première Guerre mondiale où il a fait cinq mille morts et quinze mille rescapés, et il a laissé aux victimes des séquelles à vie dans les cas les plus graves. Son utilisation a aussi été prouvée par l'Organisation pour l'interdiction des armes chimiques (OIAC) lors de la guerre civile syrienne contre les forces rebelles à Douma en 2018.
Propriétés
Le dichlore a la propriété de décolorer la solution d'indigo et plusieurs autres substances organiques. La couleur de plusieurs colorants organiques vient des différences entre les nombreux niveaux d’énergie de leurs liaisons conjuguées. Or le dichlore oxyde les doubles liaisons carbone-carbone qui constituent les systèmes de liaisons conjuguées.
Références
- CHLORE, Fiches internationales de sécurité chimique
- Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Robert H. Perry et Donald W. Green, Perry's Chemical Engineers' Handbook, États-Unis, McGraw-Hill, 1997, 7e éd., 2400 p. (ISBN 0-07-049841-5), p. 2-50.
- (en) William M. Haynes, CRC Handbook of Chemistry and Physics, Boca Raton, CRC Press/Taylor & Francis, 1er juillet 2010, 91e éd., 2610 p. (ISBN 9781439820773, présentation en ligne), p. 14-40.
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, Boca Raton, CRC Press/Taylor & Francis, 3 juin 2009, 90e éd., 2804 p. (ISBN 9781420090840, présentation en ligne).
- (en) David R. Lide, CRC Handbook of Chemistry and Physics, Boca Raton, CRC Press/Taylor & Francis, 17 juin 2008, 89e éd., 2736 p. (ISBN 9781420066791, présentation en ligne), p. 10-205.
- « The Molecular Iodine (I2) Crystal Structure (A14) », sur cst-www.nrl.navy.mil (consulté le 17 décembre 2009).
- Numéro index 017-001-00-7 dans le tableau 3.1 de l'annexe VI du règlement CE no 1272/2008 (16 décembre 2008).
- « Chlore » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 25 avril 2009.
- « Chlorine », sur hazmap.nlm.nih.gov (consulté le 14 novembre 2009).
- « Dossier : L’Eau de Javel - Solution aqueuse d’hypochlorite de sodium » , Chambre syndicale nationale de l’eau de Javel, mai 2010, p. 8, § 7 : Sécurité pour l'homme, sur eaudejavel.fr.
- « Expositions individuelles et collectives aux vapeurs de chlore », Centre Antipoisons belge.
- « Les gaz : 22 avril 1915 à Ypres (Belgique) », sur La Grande Guerre.
- « Syrie : du chlore a été utilisé contre la ville de Douma en 2018, selon l’OIAC », Le Monde.fr, 1er mars 2019 (lire en ligne, consulté le 4 octobre 2022).
- Chimie, terminale S obligatoire, programme 2002, Nathan, coll. « Sirius », 2008, 351 p. (ISBN 978-2-09-172496-6), p. 248.