Sulfure de diméthyle
Dans cet article, nous explorerons le monde fascinant de Sulfure de diméthyle, un sujet qui a retenu l'attention de personnes de tous âges et de tous intérêts. Connu pour son impact sur la société et la culture, Sulfure de diméthyle a fait l'objet de débats et d'analyses dans de nombreux domaines. Depuis son émergence jusqu'à nos jours, Sulfure de diméthyle a laissé une marque significative dans l'histoire et son influence continue d'être palpable dans le monde contemporain. A travers cet article, nous approfondirons les aspects les plus pertinents de Sulfure de diméthyle, en analysant son importance, ses implications et sa projection dans le futur. Préparez votre esprit à un voyage de découverte et d'introspection dans le merveilleux univers de Sulfure de diméthyle.
| Sulfure de diméthyle | |

| |
| Identification | |
|---|---|
| Nom UICPA | sulfure de diméthyle |
| Synonymes |
DMS |
| No CAS | |
| No ECHA | 100.000.770 |
| No CE | 200-846-2 |
| No FEMA | 2746 |
| SMILES | |
| InChI | |
| Apparence | liquide incolore à l'odeur caractéristique[1] |
| Propriétés chimiques | |
| Formule | C2H6S [Isomères] |
| Masse molaire[3] | 62,134 ± 0,007 g/mol C 38,66 %, H 9,73 %, S 51,61 %, |
| Moment dipolaire | 1,45 D[2] |
| Diamètre moléculaire | 0,481 nm[2] |
| Propriétés physiques | |
| T° fusion | −98 °C[1] |
| T° ébullition | 37,3 °C[1] |
| Solubilité | dans l'eau : nulle[1] |
| Paramètre de solubilité δ | 18,5 J1/2·cm-3/2 (25 °C)[2] |
| Masse volumique | 0,85 g·cm-3[1]
|
| T° d'auto-inflammation | 205 °C[1] |
| Point d’éclair | −49 °C[1] |
| Limites d’explosivité dans l’air | 2,2–19,7 %vol[1] |
| Pression de vapeur saturante | à 20 °C : 53,2 kPa[1]
|
| Point critique | 55,3 bar, 229,85 °C[5] |
| Thermochimie | |
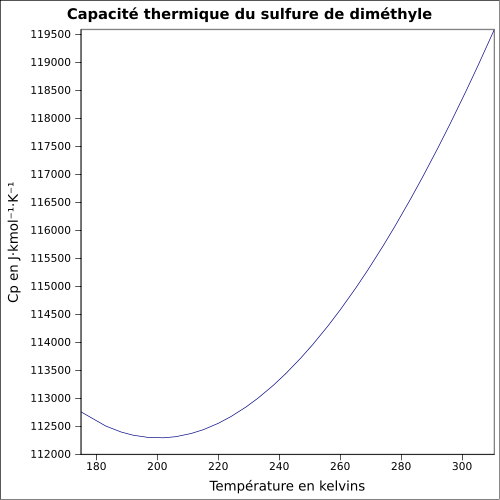
| Cp | |
| Propriétés électroniques | |
| 1re énergie d'ionisation | 8,69 ± 0,02 eV (gaz)[7] |
| Constante diélectrique | 6,70[7] |
| Propriétés optiques | |
| Indice de réfraction | 1,432[2] |
| Précautions | |
| SIMDUT[8] | |
  B2, D2B, |
|
| NFPA 704 | |
| Transport[9] | |
| Écotoxicologie | |
| LogP | 0,84[1] |
| Seuil de l’odorat | bas : 0,009 8 ppm haut : 0,02 ppm[10] |
| Unités du SI et CNTP, sauf indication contraire. | |
| modifier |
|
Le sulfure de diméthyle ou diméthylsulfure (DMS) est un composé organosulfuré de formule (CH3)2S. C'est un liquide volatil, inflammable, insoluble dans l'eau et dont la caractéristique principale est une odeur très désagréable à haute concentration. Il apparaît notamment lors de la cuisson de certains végétaux comme le maïs, le chou ou la betterave. Il est également le signe d'une infection bactérienne dans le brassage. C'est un produit de la décomposition du diméthylsulfoniopropionate (DMSP). Il est également produit par le métabolisme bactérien du méthanethiol (CH3SH), notamment dans les flatulences[11].
Sources naturelles

Le DMS est le plus abondant des composés biologiques contenant du soufre émis dans l'atmosphère[12].
Les émissions océaniques jouent un rôle important dans le cycle du soufre. Elles sont principalement issues du métabolisme et de la décomposition du phytoplancton, le DMS est injecté dans l'atmosphère via les embruns marins ou le dégazage.
Sur les continents, du DMS est également produit naturellement par la transformation bactérienne, dont dans les réseaux d'égouts, de déchets contenant du diméthylsulfoxyde (DMSO). Ce phénomène peut conduire à des problèmes environnementaux malodorants[13].
Le sulfure de diméthyle a été détecté sur Mars dans des échantillons prélevés dans le cratère Gale par le rover Curiosity[14] et dont le contenu organique évoque le kérogène terrestre[15].
Le JWST en a détecté sur l'exoplanète K2-18b[16].
Devenir dans l'atmosphère
Le DMS est oxydé dans l'atmosphère en une grande variété de composés sulfurés comme le dioxyde de soufre, le diméthylsulfoxyde (DMSO), l'acide sulfonique et l'acide sulfurique[17].
Liens avec le climat
Parmi les composés soufrés provenant de l'oxydation du DMS, l'acide sulfurique a la capacité de former de nouveaux aérosols (dits secondaires) qui peuvent agir comme des noyaux de condensation de nuages[18]. Le DMS est la principale source naturelle de sulfates et une source majeure de noyaux de condensation de nuages (CCN) dans l'atmosphère. Selon Charlson et al. (1987), son oxydation joue un rôle majeur dans une boucle de rétroaction climatique et permet ainsi de corréler la production du DMS par le phytoplancton marin et l'albédo nuageuse[18]. Cette hypothèse, connue sous le nom d'hypothèse CLAW, a eu un grand impact sur la recherche en science de l'atmosphère mais a depuis été remise en cause[19].
Par cette influence sur la formation des nuages, la présence massive et les variations naturelles ou anthropiques de DMS dans l'atmosphère océanique et subcontinentale pourrait avoir un impact significatif sur le climat global de la Terre[20].
Odeur
Le DMS a une odeur très caractéristique de chou cuit, qui peut être très incommodante à haute concentration. Son seuil de perception olfactive est très bas : il varie entre 0,02 et 0,1 ppm selon les individus. Il est cependant disponible en tant qu'additif alimentaire servant, en très faible quantité, à donner du goût (arôme alimentaire).
La betterave[21], le chou, le maïs, les asperges[22],[23],[24] et les fruits de mer dégagent du DMS lors de leur cuisson, de même que certains aliments fermentés (fromages, bières et vins)[25]. Le phytoplancton produit lui aussi du DMS. Andrew Johnston (université d'East Anglia) a caractérisé l'odeur du DMS comme l'« odeur de la mer »[26]. Il serait plus précis de dire que le DMS est un composant de l'odeur de la mer, un autre étant les phéromones (dictyoptérènes) de certaines algues. Le DMS est également un composé émis par le procédé kraft de transformation du bois en pâte à papier et par l'oxydation de Swern.
On sait depuis 1995 que le DMS libéré par le phytoplancton quand il est mangé par le zooplancton attire les Procellariiformes (les oiseaux de mer à narines tubulaires, dont les albatros, les pétrels et les puffins), eux-mêmes consommateurs de zooplancton[27],[28]. On suspecte que les baleines à fanons (dont les baleines à bosse, les baleines bleues et les rorquals) repèrent les concentrations de krill de la même façon[27].
Applications industrielles
Il est utilisé en raffinage et en pétrochimie pour contrôler la formation de coke et de monoxyde de carbone. Il est employé dans plusieurs synthèses organiques et est un sous-produit de l'oxydation de Swern. Il est également utilisé dans des arômes alimentaires, pour donner du goût. Il peut aussi être oxydé en diméthylsulfoxyde (DMSO), utilisé notamment pour ses qualités de solvant. Le plus gros producteur de DMS est l'entreprise Gaylord Chemical Corporation (en), un maillon important de l'industrie papetière à Bogalusa en Louisiane.
Sécurité
Le DMS est volatil, inflammable, irritant et a une odeur déplaisante même à faible concentration.
Cycle du soufre
Robert Charlson, James Lovelock, Meinrat Andreae et Stephen Warren font de cette molécule un élément important du cycle du soufre et de la régulation du climat dans l'hypothèse CLAW.
Notes et références
- SULFURE DE DIMETHYLE, Fiches internationales de sécurité chimique
- (en) Yitzhak Marcus, The Properties of Solvents, vol. 4, Angleterre, John Wiley & Sons, , 239 p. (ISBN 0-471-98369-1)
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- (en) Robert H. Perry et Donald W. Green, Perry's Chemical Engineers' Handbook, États-Unis, McGraw-Hill, , 7e éd., 2400 p. (ISBN 0-07-049841-5), p. 2-50
- ↑ (en) « Properties of Various Gases »(Archive.org • Wikiwix • Archive.is • Google • Que faire ?), sur flexwareinc.com (consulté le ).
- ↑ (en) Carl L. Yaws, Handbook of Thermodynamic Diagrams : Organic Compounds C8 to C28, vol. 1, Huston, Texas, Gulf Pub. Co., , 396 p. (ISBN 0-88415-857-8)
- (en) David R. Lide, Handbook of chemistry and physics, Boca Raton, CRC, , 89e éd., 2736 p. (ISBN 978-1-4200-6679-1), p. 10-205
- ↑ « Sulfure de diméthyle » dans la base de données de produits chimiques Reptox de la CSST (organisme québécois responsable de la sécurité et de la santé au travail), consulté le 23 avril 2009
- ↑ Entrée du numéro CAS « 75-18-3 » dans la base de données de produits chimiques GESTIS de la IFA (organisme allemand responsable de la sécurité et de la santé au travail) (allemand, anglais), accès le 27 novembre 2008 (JavaScript nécessaire)
- ↑ (en) « Dimethyl sulfide », sur hazmap.nlm.nih.gov (consulté le ).
- ↑ (en) F.L. Suarez, J. Springfield, M.D. Levitt, « Identification of gases responsible for the odour of human flatus and evaluation of a device purported to reduce this odour », Gut, vol. 43, no 1, , p. 100-104
- ↑ (en) Simpson, David ; Winiwarter, Wilfried ; Börjesson, Gunnar ; Cinderby, Steve ; Ferreiro, Antonio ; Guenther, Alex ; Hewitt, C. Nicholas ; Janson, Robert ; Khalil, M. Aslam K. ; Owen, Susan ; Pierce, Tom E. ; Puxbaum, Hans ; Shearer, Martha ; Skiba, Ute ; Steinbrecher, Rainer ; Tarrasón, Leonor ; Öquist, Mats G., « Inventorying emissions from nature in Europe », Journal of Geophysical Research, vol. 104, no D7, , p. 8113–8152 (DOI 10.1029/98JD02747)
- ↑ (en) Glindemann, D., Novak, J., Witherspoon, J., « Dimethyl Sulfoxide (DMSO) Waste Residues and Municipal Waste Water Odor by Dimethyl Sulfide (DMS): the North-East WPCP Plant of Philadelphia », Environmental Science and Technology, vol. 40, no 1, , p. 202–207 (DOI 10.1021/es051312a S0013-936X(05)01312-X)
- ↑
- ↑ (en) Paul Voosen, « NASA rover hits organic pay dirt on Mars », sur sciencemag.org, (consulté le ).
- ↑ « Y a t'il [sic] de la vie sur l'exoplanète K2-18b ? Peut-être... », sur ici, par France Bleu et France 3 (consulté le ).
- ↑ (en) Lucas, D.D. ; Prinn, R.G., « Parametric sensitivity and uncertainty analysis of dimethylsulfide oxidation in the clear-sky remote marine boundary layer », Atmospheric Chemistry and Physics, vol. 5, , p. 1505–1525
- Suhre, K. (1994), Modélisation couplée du transport et de la chimie du diméthyl de soufre dans la couche limite marine nuageuse. Impact climatique et étude de processus, thèse de doctorat, 220 p., 108 réf. bibl. (résumé)
- ↑ (en) P. K. Quinn et T. S. Bates, « The case against climate regulation via oceanic phytoplankton sulphur emissions », Nature, vol. 480, no 7375, , p. 51–56 (ISSN 0028-0836 et 1476-4687, DOI 10.1038/nature10580, lire en ligne, consulté le )
- ↑ (en) Malin, G. ; Turner, S.M. ; Liss, P.S., « Sulfur: The plankton/climate connection », Journal of Phycology, vol. 28, no 5, , p. 590–597
- ↑ (en) Thomas H. Parliment, Michael G. Kolor et Il Y. Maing, « Identification of the major volatile components of cooked beets », J. Food Science, vol. 42, no 6, p. 1592-1593, novembre 1977, DOI 10.1111/j.1365-2621.1977.tb08434.x (résumé)
- ↑ (de) K. H. Ney et W. Freytag (trad. Le sulfure de diméthyle comme composant essentiel de l'arôme des asperges. Études complémentaires sur les composants volatils des asperges cuites.), « Dimethylsulfid als wesentliche komponente des spargelaromas weitere untersuchungen der flüchtigen bestandteile des gekochten spargels », Springer Science and Business Media LLC, vol. 149, no 3, , p. 154–155 (ISSN 0044-3026, DOI 10.1007/bf02215685)
- ↑ Roland Tressl, Daoud Bahri, Maria Holzer et Tibor Kossa, « Formation of flavor components in asparagus. 2. Formation of flavor components in cooked asparagus », American Chemical Society (ACS), vol. 25, no 3, , p. 459–463 (ISSN 0021-8561, DOI 10.1021/jf60211a048)
- ↑ Detlef Ulrich, Edelgard Hoberg, Thomas Bittner, Werner Engewald et Kathrin Meilchen, « Contribution of volatile compounds to the flavor of cooked asparagus », Springer Science and Business Media LLC, vol. 213, no 3, , p. 200–204 (ISSN 1438-2377, DOI 10.1007/s002170100349)
- ↑ Sophie Landaud, Sandra Helinck et Pascal Bonnarme, « Formation of volatile sulfur compounds and metabolism of methionine and other sulfur compounds in fermented food », Springer Science and Business Media LLC, vol. 77, no 6, , p. 1191–1205 (ISSN 0175-7598, DOI 10.1007/s00253-007-1288-y)
- ↑ (en) Université d'East Anglia, « Cloning the smell of the seaside » (communiqué de presse), 2 février 2007
- Kate Wong, « Dans le secret des balaines », Pour la science, no 549, , p. 24-33.
- ↑ (en) Gabrielle A. Nevitt, Richard R. Veit et Peter Kareiva, « Dimethyl sulphide as a foraging cue for Antarctic Procellariiform seabirds », Nature, vol. 376, , p. 680-682 (DOI 10.1038/376680ao).
Voir aussi
Articles connexes
Liens externes
- Merzouk, Anissa, Contrôle des variations à court terme de la production biologique de diméthylsulfure (DMS) en milieu marin, thèse, .
Bibliographie
- Savoca, M. S., & Nevitt, G. A. (2014). Evidence that dimethyl sulfide facilitates a tritrophic mutualism between marine primary producers and top predators. Proceedings of the National Academy of Sciences, 111(11), 4157-4161.