Hème
 Structure de l’hème b.
Structure de l’hème b.
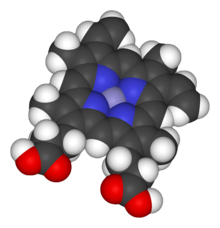 Modélisation 3D de l’hème b.
Modélisation 3D de l’hème b.
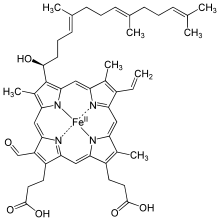 Structure de l’hème a.
Structure de l’hème a.
L’hème est un cofacteur contenant un atome de métal, souvent du fer, servant à accueillir un gaz diatomique (par exemple du dioxygène O2) au centre d’un large anneau organique appelé porphyrine. Toutes les porphyrines ne contiennent pas nécessairement un atome de fer mais la majorité des métalloprotéines qui contiennent des porphyrines ont en fait l’hème comme sous-unité prosthétique.
Il existe trois types d’hème biologiquement importants :
- l’hème b est le type d’hème le plus commun. L’hémoglobine et la myoglobine sont des exemples de protéines qui contiennent de l’hème b. L’hème b n’a pas de liaison covalente avec l’apoprotéine, étant coordonné à celle-ci par son cation ferreux ;
- l’hème a diffère de l’hème b en ce que sa chaîne latérale méthyle en position 18 est oxydée en aldéhyde et que sa chaîne latérale vinyle en position 3 est remplacée par un terpénoïde. Comme l’hème b, l’hème a n’est pas lié par covalence avec l’apoprotéine. Un exemple de protéine contenant de l’hème a est la cytochrome c oxydase ;
- l’hème c diffère de l’hème b en ce que les deux chaînes latérales vinyle sont liées par covalence à la protéine elle-même. Le cytochrome c et le complexe bc1 sont des exemples de protéines qui contiennent de l’hème c.
D’une manière générale, le nom des cytochromes tend à refléter — mais ce n’est pas une règle stricte — le type d’hème qu’ils contiennent. Ainsi, le cytochrome a contient de l’hème a, le cytochrome c contient de l’hème c.
| Hème a | Hème b | Hème c | Hème o | ||
|---|---|---|---|---|---|
| No CAS | 18535-39-2 | 14875-96-8 | 26598-29-8 | 137397-56-9 | |
| PubChem | 5288529 | 444097 | 444125 | 15719509 | |
| Formule brute | C49H62FeN4O6 | C34H32FeN4O4 | C34H36FeN4O4S2 | C49H58FeN4O5 | |

|
Groupe fonctionnel en C3 | –CHOH–CH2–Far | –CH=CH2 | –CH(cystéin-S-yl)CH3 | –CHOH–CH2–Far |
| Groupe fonctionnel en C8 | –CH=CH2 | –CH=CH2 | –CH(cystéin-S-yl)CH3 | –CH=CH2 | |
| Groupe fonctionnel en C18 | –CH=O | –CH3 | –CH3 | –CH3 | |
Voir aussi
 Portail de la chimie
Portail de la chimie  Portail de la biochimie
Portail de la biochimie  Portail de la biologie cellulaire et moléculaire
Portail de la biologie cellulaire et moléculaire  Portail de l’hématologie
Portail de l’hématologie